کاربردهای تیتانیوم در پزشکی و دندانپزشکی
تیتانیوم در کاربردهای ارتوپدی برای اولین بار در دهه 50 میلادی مورداستفاده قرار گرفت. ارتوپدی شاخهای از جراحی است که مربوط به سیستم اسکلتی-عضلانی میشود. جراحان ارتوپدی از هر دو روش جراحی و غیر جراحی برای معالجه آسیبهای اسکلتی-عضلانی، بیماریهای ستون فقرات، آسیبهای ورزشی و موارد دیگر استفاده میکنند. تیتانیوم همچنین در کاربردهای قلبی-عروقی مورداستفاده قرار میگیرد (مربوط به قلب و رگهای خونی در بدن). رگهای خونی مواد غذایی و اکسیژن را به بافتهای بدن منتقل میکنند و دیاکسید کربن و سایر ضایعات را خارج میکند. رگها در معرض تعدادی بیماری ازجمله تصلب شرایین (سخت شدن رگها)، بیماری عروق کرونر، ناراحتی دریچه قلب و موارد دیگر قرار دارند.
بدن انسان بهراحتی تیتانیوم را میپذیرد؛ ثابت شده است که زیست سازگارتر از فولاد زنگ نزن یا کروم کبالت است. علاوه بر این، تیتانیوم دارای مقاومت خستگی بالاتری نسبت به بسیاری از فلزات دیگر است. همچنین با MRI (تصویربرداری با رزونانس مغناطیسی) و CT (فناوری محاسباتی) سازگار است که در تبدیل آن به عنوان یک ماده موردنظر در کاربردهای ارتوپدی نیز کمک میکند.
هرسال بیش از 1000 تن (2.2 میلیون پوند) تیتانیوم در بیمارانِ سراسر جهان کاشته میشود و قرار است با طولانیتر شدن زندگی مردم، یا آسیب جدی در ترافیک جادهای یا حوادث دیگر، افزایش یابد. تیتانیوم سبک، مستحکم و کاملاً زیست سازگار است؛ که آن را یکی از معدود موادِ در حال حاضر شناختهشدهای میسازد که بهطور طبیعی با الزامات کاشت در بدن انسان مطابقت دارد. ازآنجاکه تیتانیوم در برابر خوردگی مقاومت میکند، زیست سازگار است و توانایی ذاتی در اتصال به استخوان انسان را دارد، به یکی از پایههای اصلی درزمینههای پزشکی تبدیلشده است. از تجهیزات جراحی تیتانیوم گرفته تا میلهها، میخها و صفحات ارتوپدی تیتانیومی، تیتانیوم به ماده اساسی مورداستفاده در پزشکی تبدیلشده است. تیتانیوم در خارج از پزشکی نیز بسیار مورداستفاده قرار میگیرد. تیتانیوم برای بسیاری از صنایع مختلف ازجمله دنیای خودرو، هوافضا و معماری نیز بسیار مفید است.
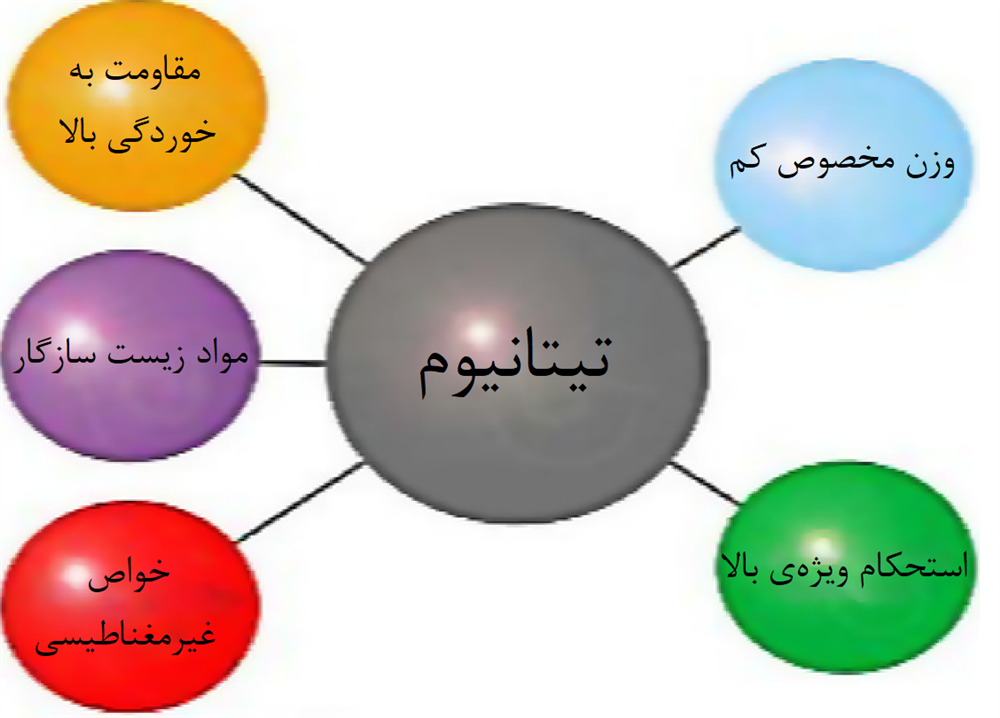
شکل 1-1-1 ویژگیهای تیتانیوم که آن را برای کاربردهای پزشکی و دندانپزشکی جذاب میکند.
شکل 1-1-2 داربست Ti-6Al-4V برای کاربردهای ایمپلنتهای پزشکی ساختهشده با استفاده از فناوری ساختِ افزایشی با لیزرِ ذوب انتخابی.
شکل 1-1-3 رفتار خوردگی کلی تیتانیوم با خلوص تجاری و آلیاژهای Ti-Pd در مقایسه با سایر فلزات و آلیاژها در اسیدهای اکساینده و احیایی؛ در حضور و عدم حضور یونهای کلرید.
بهطورکلی، هر فلز یا آلیاژ برای محیطهای زیر خطوط مربوطهاش قابلاستفاده است.
شکل 1-1-4 تیتانیوم برخلاف آهن بسیار مقاوم در برابر خوردگی است [4].
ایمپلنتهای تیتانیومی بدن
ایمپلنت باید در کاربردهای بحرانیای به صورت دائمی قرارگیرد که در آن امکان نگهداری یا تعویض سریع وجود ندارد. از این نظر وضعیت چالشبرانگیزتری از ایمپلنتهای بدن انسان وجود ندارد. در اینجا، اثربخشی و قابلیت اطمینان ایمپلنتها و تجهیزات پزشکی و جراحی از عوامل اساسی در نجات زندگی و تسکین طولانیمدت رنج و درد است. ایمپلنت کردن نشاندهنده یک ضربهی قوی به ساختار شیمیایی، فیزیولوژیکی و مکانیکی بدن انسان است. در بافت زنده هیچچیز قابلمقایسه با ایمپلنت فلزی وجود ندارد. بیشتر فلزات در مایعات و بافتهای بدن در کمپلکسهای آلی پایدار یافت میشوند. خوردگی فلز ایمپلنت شده توسط مایعات بدن منجر به آزاد شدن یونهای فلزی ناخواسته با تداخل احتمالی در فرآیندهای زندگی میشود. برای سرکوب واکنش بدن در برابر فلزات سمی یا عناصر حساسیتزا مانند نیکل، مقاومت به خوردگی بهتنهایی کافی نیست و حتی غلظتهای بسیار کم ناشی از حداقل خوردگی، ممکن است باعث عملیات پسزدگی شود. به نظر میرسد که تیتانیوم نسبت به کلیه مایعات و بافتهای بدن در برابر خوردگی مصون است و ازاینرو کاملاً زیست سازگار است.
دلایل انتخاب تیتانیوم برای ایمپلنت، ترکیبی از مطلوبترین خصوصیات ازجمله ایمنی در برابر خوردگی، زیست سازگاری، استحکام، مدول و چگالی کم و ظرفیت اتصال به استخوان و بافتهای دیگر (پیوند استخوان) است. ترکیب خواص مکانیکی و فیزیکی آلیاژهای تیتانیوم، آنها را برای تهیه ایمپلنتهایی که بسیار آسیبپذیر هستند آماده میسازد. آناتومی انسان بهطور طبیعی، شکل و حجم مجاز ایمپلنت را محدود میکند. مدول پایین آلیاژهای تیتانیوم در مقایسه با فولاد عامل مثبت در کاهش جذب مجدد استخوان است. دو پارامتر دیگر، سودمندی آلیاژ ایمپلنت را تعریف میکند، حساسیت به شکاف (بهعنوانمثال، نسبت استحکام کششی در حالت شکاف دار به حالت بدون شکاف) و مقاومت در برابر انتشار ترک، یا چقرمگی شکست. تیتانیوم در هر دو مورد بهخوبی نمره میگیرد. نسبتهای NS/TS معمولی برای تیتانیوم و آلیاژهای آن 1.4-1.7 است (برای مواد ایمپلنت قابلقبول حداقل 1.1 است). چقرمگی شکست آلیاژهای استحکام-بالایی که قابلیت ایمپلنت شدن دارند، بالای MPa.m-½ 50 است که طول ترک بحرانی بسیار بالاتر از حداقل طولِ قابلتشخیص با روشهای استاندارد تستهای غیر مخرب دارند. نمونههایی از تیتانیوم استفادهشده در ایمپلنتهای بدن در شکلهای 1-1-5 تا 1-1-7 نشان دادهشده است و استفادههای دندانپزشکی آن بعداً در این بخش توضیح داده میشود.
برای کاربردهای دندانپزشکی با استفاده از ایمپلنتهای تیتانیوم، تغییر بزرگی درترمیم دندان در سطح جهان امکانپذیر شد. ریشه تیتانیوم در استخوان فک وارد میشود و باگذشت زمان اجازه پیوند استخوان داده میشود. سپس ساختار فوقانی دندان بر روی ایمپلنت ساخته میشود تا بتواند جایگزینی مؤثری داشته باشد.
تیتانیوم همچنین در جراحی ترمیم آسیبهای صورت استفاده میشود. استفاده از بافت خود بیمار همیشه نمیتواند نتایج مطلوب را به دست آورد. ممکن است برای بازیابی توانایی صحبت کردن یا غذا خوردن و همچنین زیبایی ظاهری صورت اجزای مصنوعی به کار رود تا ویژگیهای ازدسترفته در اثر آسیبدیدگی یا بیماری را جایگزین کند. ایمپلنتهای پیوند استخوان تیتانیوم که تمامی نیازهای زیست سازگاری و استحکام را برآورده میکند، پیشرفتهای بیسابقهای را در عمل جراحی برای درمان موفقیتآمیز بیماران مبتلابه نقصهای بزرگ و شرایط بسیار مشکلساز فراهم آورده است.
مقاله جامعی با عنوان «یادگیری ایمپلنتهای جایگزین زانو و مفصل ران» در مجله انجمن بینالمللی تیتانیوم فصل دوم، 2016 نسخه پزشکی منتشر شد [5]. این مقاله نشان داد که جایگزین زانوی تیتانیوم میتواند متناسب با اندازه، وزن و جنسیت بیمار ساخته شود (یک زن از ساختار استخوانی باریکتری برخوردار است، بهخصوص در استخوان ران). مقاله همراه آن [5، ص 20] در مورد تأثیر پردازش (بهویژه، شرایط اچ شده در مقابل شرایط اچ نشده) در شکلگیری پروتزهای تیتانیوم گوش میانی بحث میکند، شرایط اچ شده عملکرد بهتری نشان میدهد. مقاله دیگری [5، ص 76] جزئیات مربوط به ایمپلنت مفصل ران تیتانیوم تولیدشده توسط چاپ 3 بعدی با یک فنجان کاملاً متخلخل را نشان میدهد (شکل 1-1-8) که امکان رشد استخوان و بافت را فراهم میکند و درنتیجه عملکرد عالی خواهد داشت. ایمپلنت قفسه دنده و جناغ ساختهشده به روش ساخت افزایشی در شکل 1-1-9 A و B نشان دادهشده است [5، ص 82]. شکل 1-1-10 یک سیستم ترمیم کنترل مدفوع تشکیلشده از یک سری دانههای تیتانیوم با هستههای مغناطیسی متصل به سیمهای تیتانیوم برای تشکیل یک حلقه را نشان دادهشده است [5، ص 83].
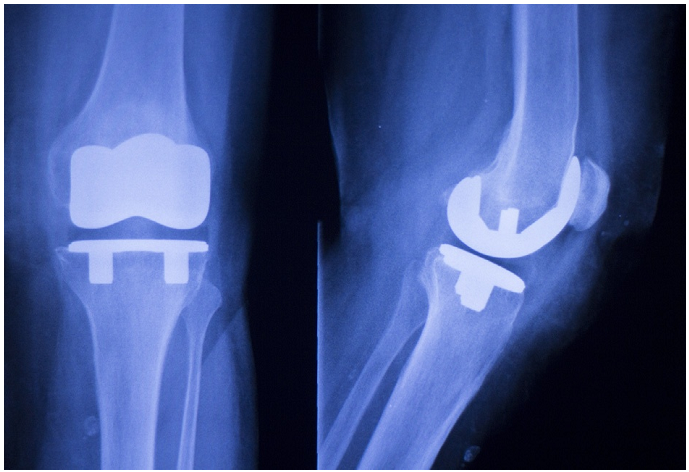
شکل 1-1-5 اشعه ایکس نشاندهندهی ایمپلنت جایگزین مفصل زانو در اسکن پزشکی آسیبشناسی ارتوپدی
شکل 1-1-6 ایمپلنت استخوان تیتانیومی
شکل 1-1-7 یک ایمپلنت سنتی جایگزین مفصل ران
شکل 1-1-8 اسمیت و نفیو (اسامی دانشمندان) کاپ کاملاً متخلخل با فنآوری کنسلوک را اصلاح کردند
(با تشکراز پروفسور ه. پ. تانگ، آزمایشگاه کلیدی ایالتی مواد فلزی متخلخل، مؤسسه شمال غربی تحقیقات فلزات غیر آهنی)
شکل 1-1-9 (A) ایمپلنت قفسه دنده و جناغ ساختهشده به روش ساخت افزایشی سهبعدی
(B) چگونگی قرار گرفتن جز A در بدن انسان نشان دادهشده است
شکل 1-1-10 سیستم ترمیم کنترل مدفوع تیتانیومی
یک استخوان فک ساختهشده به روش ساخت افزایشی در شکل 1-1-11 نشان دادهشده است [4].
کار جالب دیگری شامل مطالعه آلیاژهای Ti-Au بود [6]. آلیاژ متشکل از 1:3 Ti:Au (شکل 1-1-12) سختی چهار برابر بیشتر از تیتانیوم خالص داشت و زیست سازگارتر بود و مقاومت در برابر سایش بهتری داشت که این آلیاژ را انتخابی جذاب برای کاربردهای ایمپلنت ساخت.
شکل 1-1-11 یک استخوان فک ساختهشده با روش ساخت افزایشی.
شکل 1-1-12 ساختار کریستالی بتا تیتانیوم-3 طلا (با احترام از ای. مروسان، دانشگاه رایس).
ایمپلنتهای دندانی تیتانیومی
استفاده از تیتانیوم در کاربردهای دندانپزشکی نیز به طرز چشمگیری طی 20 سال گذشته افزایشیافته است. جایگزین دندانهای ازدسترفته با پروتزهای پشتیبانی شده با ایمپلنت، نشان دادهشده در شکلهای 1-1-13 و 1-1-14 [4]، بهطور گستردهای در دندانپزشکی برای توانبخشی بیمارانِ کاملاً و یا جزئی بیدندان پذیرفتهشده است. این پیشرفت در توانبخشی دهان و دندان مبتنی بر مفهوم استخوانسازی است. این پدیدهی بیولوژیکی بهعنوان قرارگیری مستقیم استخوان بر روی سطح ایمپلنت تیتانیوم توصیفشده است. در حال حاضر، تیتانیوم خالص تجاری (CP) بهعنوان مادهی ایمپلنت دندانی انتخابشده است، زیرا دارای خواص بیولوژیکی و بیومکانیکی عالی است.
شکل 1-1-13 کاشت دندان تیتانیوم (بالا) و قرار دادن آنها به دهان (پایین)
تجهیزات جراحی تیتانیومی
طیف گستردهای از تجهیزات جراحی از تیتانیوم ساختهشدهاند (به شکل 1-1-15 تا 1-1-17 نگاه کنید [4]). یکی از مزایای آن در این رابطه، سبک بودن آن است که به کاهش خستگی جراح کمک میکند. تجهیزات برای تهیهی سطح غیر منعکسکننده که در جراحیهای میکروسکوپی مانند جراحی چشم ضروری است، بهطور مکرر آنودایز میشوند. تجهیزات تیتانیومی میتوانند بدون تخریب لبه یا کیفیت سطح، مقاومت در برابر خوردگی و استحکام بهطور مکرر استریل شوند. تیتانیوم غیر مغناطیسی است، بنابراین تهدیدی برای آسیب وسایل الکترونیکی ایمپلنت شده، کوچک و حساس وجود ندارد.
شکل 1-1-15 تجهیزات جراحی تیتانیومی، قیچیها، انبرکها و نگهدارندههای سوزن
شکل 1-1-16 تجهیزات تیتانیومی، پیچهای جراحی و ایمپلنتهای مختلف
شکل 1-1-17 تجهیزات تیتانیومی دیگر
تیتانیوم در صندلیهای چرخدار و دیگر تجهیزات پزشکی
همین خصوصیاتی که تیتانیوم را انتخابی مناسب برای ایمپلنتها و تجهیزات میسازد، آن را انتخاب خوبی خصوصاً به شکل لولهای (شکل 1-1-18 A و B [4]) برای صندلیهای چرخدار (شکل 1-1-19 [4]) و واکرها (شکل 1-1-20 [4]) میسازد. محصولات لولهای بهطورکلی چه بهعنوان اجزای یکپارچه، چه جوش دادهشده از تیتانیوم خالص تجاری یا آلیاژ Ti-3Al-2.5 V ساخته میشوند.
شکل 1-1-18 (A) لوله تیتانیومی
(B) لوله تیتانیومی آماده استفاده در صندلی چرخدار یا واکر
شکل 1-1-19 (A، B) تیتانیوم یک انتخاب محبوب برای صندلیهای چرخدار است
شکل 1-1-20 واکر تیتانیومی
مشخصات تیتانیوم در کاربردهای پزشکی و دندانپزشکی
برگهها و مشخصات مواد در تعدادی از استانداردهای بینالمللی و داخلی، ازجمله ASTM و BS7252/ISO 5832، همانطور که در جدول 1-1-1 نشان دادهشده، شرح دادهشده است [2]. آلیاژهایی مانند Ti-6Al-7Nb استفاده از V را از بین میبرد، عنصری که میتواند منجر به آزاد شدن سم سلولی شود (تأثیر منفی بر روی سلولهای انسانی به شیوهای مشابه با اثر زهر پف افزودنی).
خصوصیات مکانیکی آلیاژهای تیتانیوم مناسب برای استفاده در کاربردهای پزشکی و دندانپزشکی در جدول 1-1-2 نشان داده شده است.
|
ASTM
|
BS/ISO
|
تعیین آلیاژ (ها)
|
|
F67
|
بخش 2
|
تیتانیوم غیر آلیاژی___خلوص تجاری سطح 1-4 (ASTM F1341 سیم را مشخص میکند)
|
|
F136
|
بخش 3
|
Ti6Al4V ELI کارشده (ASTM F620، ELI فورج شده را مشخص میکند)
|
|
F1472
|
بخش 3
|
Ti6Al4V سطح استاندارد (SG) کارشده (F1108، SG ریختگی را مشخص میکند)
|
|
F1295
|
بخش 11
|
Ti6Al7Nb کارشده
|
|
_
|
بخش 10
|
Ti5Al2.5Fe کارشده
|
|
F1580
|
_
|
پودرهای خالص تجاری و سطح استاندارد Ti6Al4V برای پوشش ایمپلنتها
|
|
F1713
|
_
|
Ti13Nb13Zr کارشده
|
|
F1813
|
_
|
Ti12Mo6Zr2Fe کارشده
|
جدول 1-1-1 مشخصات تیتانیوم در کاربردهای پزشکی و دندانپزشکی
|
|
سطح ASTM
|
|
ویژگی
|
1
|
2
|
3
|
4
|
5
|
|
استحکام تسلیم (Mpa)
|
170
|
275
|
380
|
483
|
795
|
|
کشش نهایی
|
240
|
345
|
450
|
550
|
860
|
|
استحکام (MPa)
|
|
|
|
|
|
|
ازدیاد طول (%)
|
24
|
20
|
18
|
15
|
10
|
|
مدول الاستیک (GPa)
|
103-107
|
103-107
|
103-107
|
103-107
|
114-120
|
جدول 1-1-2 آلیاژهای تیتانیوم مناسب برای کاربردهای پزشکی
اقتباس از ASTM F67 (درجه 1 تا 4) و F136 (درجه 5).
سایر مواد پزشکی بر پایهی تیتانیوم
نیکل تیتانیوم که بهعنوان نایتینول (بخشی از آلیاژهای حافظهدار) نیز شناخته میشود، آلیاژ فلزی نیکل و تیتانیوم است که در آن دو عنصر با درصد اتمی تقریباً مساوی وجود دارند، بهعنوانمثال، نایتینول 55، نایتینول 60. آلیاژهای نایتینول دو خاصیت نزدیک به هم و منحصربهفرد ارائه میدهند: اثر حافظهداری (SME) و سوپرالاستیسیته (SE)؛ که شبه کشسانی نیز نامیده میشود، (PE). حافظهداری، توانایی نایتینول است که در یک دما دچار تغییر شکل شود و بعد از گرم کردن تا بالاتر از «دمای استحاله»، شکل اصلی و تغییرشکلنیافتهی خود را بازیابی کند. سوپرالاستیسیته در یک محدوده دمای باریک درست بالاتر از دمای استحاله رخ میدهد. در این حالت، هیچ گرمایشی لازم نیست تا شکل تغییرشکلنیافته بازیابی شود و این ماده دارای خاصیت الاستیسیته بزرگی، حدود 10-30 برابر فلز معمولی است.
نایتینول بسیار زیست سازگار است و خواص دیگری نیز دارد که آن را برای استفاده در ایمپلنتهای ارتوپدی مناسب میکند. خواص منحصربهفرد آن باعث تقاضای زیاد در وسایل پزشکی کمتر تهاجمی شده است. لوله نایتینول معمولاً در سوندها، استنتها و سوزنهای سوپرالاستیک استفاده میشود. در جراحی کلورکتال از این ماده در دستگاههای اتصال مجدد روده پس از برداشتن آسیب استفاده میشود. نایتینول در دستگاههایی که توسط فرانتز فرویدنتال توسعهیافته برای درمان آرتریوسوس مجرای باز، مسدود شدن رگ خونی که ریهها را پشت سر میگذارد و پس از تولد در یک نوزاد بسته نشده است، استفاده میشود. در دندانپزشکی از این آلیاژ در ارتودنسی برای براکت ها و سیمهای اتصالدهنده دندان استفاده میشود. پس از قرار دادن سیم SME دردهان، دمای آن تا رسیدن به دمای بدن افزایش مییابد. این امر باعث میشود که نایتینول به حالت اولیه خود منقبض شود و یک نیروی ثابت برای حرکت دندانها اعمال کند. این سیمهای SME مانند سایر سیمها نیازی به سفت شدن مجدد ندارند زیرا برخلاف سیمهای زنگنزن معمولی، میتوانند با حرکت دندانها منقبض شوند. علاوه بر این، از نایتینول میتوان در ریشهشناسی دندان استفاده کرد، جایی که از سوهانهای نایتینول برای تمیز کردن و شکل دادن کانالهای ریشه در طی مراحل کانال ریشه استفاده میشود.
خواص غیرمعمول نایتینول برگرفته از استحاله فازی حالتجامد برگشتپذیر است که بهعنوان یک استحالهی مارتنزیتی شناخته میشود. در دماهای بالا، نایتینول یک ساختار متداخل، ساده، مکعبی که به آن آستنیت گفته میشود، به خود میگیرد. در دماهای پایین، نایتینول بهطور خودبهخود به یک ساختار کریستالی پیچیدهتر تتراگونال مرکز پر که به مارتنزیت معروف است، تبدیل میشود. معمولاً دمایی که در آن آستنیت به مارتنزیت تبدیل میشود، دمای استحاله نامیده میشود. مکانیسم اثر حافظهداری که شامل استحالهی مارتنزیت دمای پایین به آستنیت دما بالاتر است، باعث بازیابی شکل اصلی میشود (شکلهای 1-1-21 و 1-1-22 را ببینید [4]).
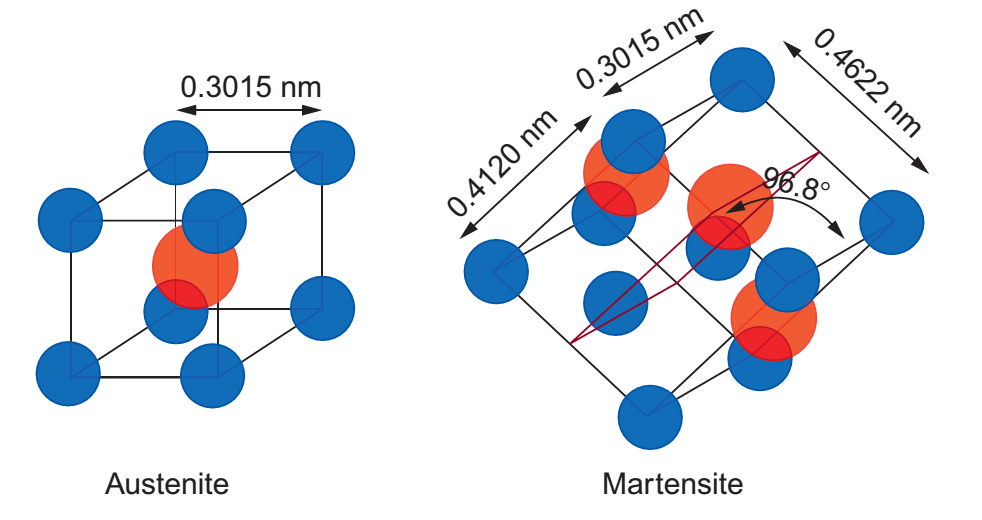
شکل 1-1-21 مکانیسم اثر حافظهداری. استحالهی مارتنزیت دمای پایین به آستنیت دما بالاتر باعث بازیابی شکل اصلی میشود
شکل 1-1-22 نمایش اثر حافظهداری
یک استنت نایتینول و نحوه عملکرد آن در شکلهای 1-1-23 و 1-1-24 [4] نشان دادهشده است.
یک دستگاه تثبیتکنندهی نایتینول در شکل 1-1-25 [4] نشان دادهشده است.
استفادهی دندانپزشکی از نایتینول در یک بست دندان در شکل 1-1-26 [4] نشان دادهشده است.
اخیراً آلیاژهای فراتر از آلیاژهای نسل اول نهایی تولیدشدهاند. اینها شامل Ti-6Al-4V، Ti-6Al-7Nb و سطحهای خالص تجاری است. این آلیاژها مدولهای کم، نزدیک بتا و آلیاژهای بتا دارند که با مدول کم استخوان انسان مطابقت دارد [8]. آلیاژهایی مانندTi-29Nb-13Ta-4.6Zr، Ti-13Nb-13Zr و Ti-10Nb-10Zr با روشهای ریختهگری تزریقی فلزات ساختهشده و از استحکام خوبی و زیست سازگاری عالی با بدن انسان برخوردار هستند.
شکل 1-1-23 یک استنت نایتینول
شکل 1-1-24 طرز کار استنت نایتینول
شکل 1-1-25 دستگاههای تثبیتکنندهی نایتینول.
شکل 1-1-26 بستهای دندانی نایتینول. (A) طرحی از بستهای قرارگرفته روی دندانها و
(B) بستهای دندانی روی دندانها.
پینوشت:
خلاصهی جامع استفاده از AM (ساخت افزایشی) در دندانپزشکی در شکل 1-1-27 نشان دادهشده است.
شکل 1.1.27 خلاصهای از کاربرد AM (ساخت افزایشی)در دندانپزشکی.
این کتاب:
این کتاب بر روی تیتانیوم در کاربردهای پزشکی و دندانپزشکی، ازجمله ایمپلنتها، تجهیزات و وسایلی مانند صندلی چرخدار و واکر تمرکز دارد. این کتاب شامل اطلاعاتی در مورد تکنیکهای مختلف ساخت ازجمله شمشریزی معمولی و پردازشهای بعدی (فورج، نورد، اکستروژن و غیره) و رویکردهایی همچون متالورژی پودر، ساخت افزایشی و قالبریزی تزریقی فلزات است. همچنین حاوی اطلاعاتی در مورد تعدادی آلیاژ است که از تیتانیوم خالص تجاری و Ti-6Al-4V شروع میشود و به ترکیباتی مانند نایتینول (ترکیبات Ti-Ni با درصد اتمی تقریباً برابر) میرسد.
[1] Titanium Industries, Inc., US office of Technical Assessment Web Page (accessed 7-07-16).
[2] AZO Materials Web Page (accessed 7-07-1)
[3] Wikipedia, (accessed 7-17-16).
[4] Internet Explorer, Titanium Implants Illustrations, vol. 8 (accessed 11-25-16).
[5] Padgett, D.E., Windsor, R.E., 2016. International Titanium Association. Titan. Today (2nd Quarter), 11.
[6] Anon, 2016. Gold boosts titanium knee strength. Adv. Mater. Process. 174 (8) 8,9.
[7] Elias, C.N., et al., 2008. Biomedical applications of titanium and its alloys. JOM (March), 46.
[8] B. Williams, Powder injection molding international, “World PM2016: PIM Technical Sessions Review Advances in Novel Titanium Alloys for Biomedical Applications.